�J���{���_���n�t�ɂ�����
�|�����_�����̌���
�Q�n���������_�э����w�Z
���@�ȁ@��
1�@�͂��߂�
�@���݁A�������̎���ɂ͗l�X�Ȋ���肪����B���̒��ŁA�����Ƃ��g�߂Ȋ����Ƃ����S�~���ł͂Ȃ����낤���B�����������͂�������̃S�~��r�o���A���̃S�~�͏ċp�����▄�ߗ��ď����ɂ���ď�������Ă���B�������A�����̏������@�ɂ͂������̖�肪����B���Ƃ��Ώċp�������s���ƁA�L�Q�Ȕr�C�K�X���o����A�n�����g���ɂȂ����_���Y�f���r�o�����B�܂����ߗ��ď����ł͂��̂܂ܓy�̒��Ɏc���Ă��܂���������A����ɖ��ߗ��Ēn�s���ŏo���ꂽ�S�~��S�����ߗ��Ă�ɂ͌��E������B
�@�������͗l�X�ȃS�~�̏������@���l���Ă��������ɐ����𐫃v���X�`�b�N�̑��݂�m�����B�����𐫃v���X�`�b�N�͔p�����ꂽ��A�����̔������̓����ɂ���ē�_���Y�f�Ɛ��ɕ�������Ă��܂����ł���B�����������𐫃v���X�`�b�N�ɂ���肪����A�����𐫂𗘗p���ĕ�����������ɂ�1�N�ȏ���̎��Ԃ�K�v�Ƃ����P�j�Q�j�B�����Ԃ�K�v�Ƃ���Ƃ������Ƃ͍L��ȏ�������K�v�ɂȂ��Ă���B�����ŁA�������̓|�����_�������Ƃ��āA�����S�~�Ƃ��Ĕr�o���ꂽ�����𐫃v���X�`�b�N��Z���Ԃŕ�������������@�̊J�������Ă����B
�@���̌��ʁA�P�X�X�W�N�V���܂łɍ������^�����y���Ƀ|�����_����u���Ă����ƕ��������܂邱�ƁA���^�����y�����P�O�O�����̍����ɂ��Ă��̒��Ƀ|�����_����u���Ă����ƕ��������܂邱�Ƃ������B�܂��A�P�X�X�X�N�T���܂łɂ̓��^�����y�����ł̕������A�_�ɂ���������̒ᕪ�q���R�j�ƁA����ɂ��\�ʂ���̒ᕪ�q�������������ɂ����Ă��邱�Ƃ����Ƃ߂��S�j�B�����ł̎_�́A���^�����y�̌��ʐ��Y�����ዉ���b�_�̂��Ƃł���B�������͂���ɁA�ዉ���b�_�ɂ��|�����_�̕����@�\�̌����ւƐi�߂��B
�Q�@���@
�Q�D�P�@����
�@�����ɂ̓t�B������̂k�|�|�����_�i�o�k�k�`�j�i�O�䓌�����w���j���g�p�����B
�@���̃|�����_�̓g�E�����R�V�Ȃǂ��������f���v���ⓜ�ނy�����ē�������_�������Ƃ��A���_�̒��ڏk���@�ɂ�萻���������������^�̐����𐫎����ł���B���ڏk���@�œ���ꂽ�����q�ʂ̃|�����_�́A�ėp�����ł���|���G�`������|���X�`�����Ɣ�r���Ă��\���ȋ��x�������Ă���B�܂��A���̐����𐫃v���X�`�b�N�ɔ�ׂč����������������Ă���A�����������ł��J�r�������Ȃ������������Ă���B
�@�����͌�����R�O�ʂ��A�V�[�g�����t���������������A�V�[�g�����c�����Ƃ��A�V�[�g�����P�P�Omm�A�c�P�Omm�ɐ�o���Ď����ЂƂ����B
�iFig.1�o�k�`�t�B�����̐�o�����@)
�Q�D�Q�@�����̕]��
�Q�D�Q�D�P�@�͊w�����̑���
�@�@���o���������Ђ���50mm�A�c10mm�ɐ�o����Fig.�Q�̎��쑪���Ŕj�f���d�𑪒肵���B�j�f���d�ƃt�B�����̕��A��������j�f���x���v�Z�����B
�Q�D�Q�D�Q�@���q�ʑ���
�@�o�k�`�̕��q�ʑ���́A�E�x���[�e�^�S�x�v�iSHIBATA29-01�j��p���ĔS�x�@�ɂ��s�����B�iFig.�R�͔S�x����̗l�q�j
�@�S�x���ϕ��q�ʂlv�͉��L�̎菇�ŎZ�o�����B
�@
�S�x�@�ɂ�镪�q�ʑ���
�菇�P�E�n�t����
�@�N�����z�����W�O�������Ɏ��ʑ��肵���o�k�`��n�����B�@�Z�x���O
�A�@�̗n�t����Q�O�����Ƃ�N�����z�������P�O����������B �Z�x���P ���Q�^�R�E���O
�B�@�̗n�t����Q�O�����Ƃ�N�����z�������Q�O����������B �Z�x���Q ���P�^�Q�E���O
�B�@�̗n�t����P�O�����Ƃ�N�����z�������Q�O����������B �Z�x���R ���P�^�R�E���O
�@
�@�@�@�@�@�������x�R�O�O���ȏ�|�P�O�O�O���ȉ��͈̔͂ɂ����܂�悤�ɂ���B
�@�@�@�@�@�@�@�@��sp���O�D�P�`�P�D�O�ƂȂ�悤�Z�x����
�@�@�@�@�@�@�@�@��rel�����^���O���P�D�P�`�Q�D�O
�@
�菇�Q�@�n�}�̔S�x����
�@���E��������
�@�@�N�����z������A�Z�g����эnj����籽��ڰ���ŋz������������
�A�P�����@�n�}�i�N�����z�����j�̗������ԁ@�i���O�j���聨�R��̕��ϒl���O
�B���E��������
�@�@�N�����z������A�Z�g����эnj����籽��ڰ���ŋz������������
�@
�菇�R�@�n�t�̔S�x����
�@���E��������
�@�@�N�����z������A�Z�g����эnj����籽��ڰ���ŋz������������
�A�n�t�i�Z�x���@���^�����j�̗������ԁ@�i���j���聨�R��̕��ϒl��
�B���E��������
�@�@�N�����z������A�Z�g����эnj����籽��ڰ���ŋz������������
�C���O�@���P�@���Q�@���R�̂S�Z�x�ɂ��đ���
�@
�菇�S�@�f�[�^����
�@�n�}�̒ʉߎ��ԁ@���O�@�@�n�t�̒ʉߎ��ԁ@�� ����@
�@���ΔS�x��rel �iʰ����߱�Ղ̎����j�����߂��B
���P�@��rel���Ł^��0���ς��^���O���O�@�����^���O�i���Ecm-1�Esec-1�j
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@���O�A�ς͗n�}�A�n�t�̖��x
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@��0�A�ł͗n�}�A�n�t�̐�ΔS�x
�@�����q���ł̍L����A�傫��
�@�@���@�����q���n�܂ɗn�������߂ɔS�x�����ΓI�ɂǂꂾ���ς�������̊����@���@��S�x��sp
�@
�A���ΔS�x��rel �����S�x��sp�@�����߂��B
���Q�@��sp���@�i�Ł|��0�j�^ ��0 ����rel�|�P
�B�Z�x�������Ȃ�قǔ�S�x��sp �͑傫���Ȃ�B������100ml�i�Pdl�j���ɂP���n�������Ƃ��̔�S�x�ɂ��邽�߂ɁA��S�x��sp��Z�x���@g�^dl�Ŋ����ĊҌ��S�x�i���Z�S�x�j��red�����߂�B
���R�@��red����sp�^��
�@�@�@�@�Ҍ��S�x�̒P�ʂ��^dl�̈Ӗ�
�@�@�@�@�@�@�����ʂ������^�l���@�@���l�����A�l�����q�P�̎��ʁE�A�{�K�h����
�@�@�@�@�@�@�@�@�@�@�A�{�K�h�����E�������q���Ȃǂ̊W����A���^������
�@�@�@�@�@�@�@�@�@�@�̐ρ^���q�P�̎��ʁE���q���ƂȂ蕪�q�����n�t���Ő�߂��e�ς������P�ʁB
�@
�C�Ҍ��S�x��red����sp�^���@�Ɓ@���@�̃O���t������B
�@�@�O���t�̌X���������f�A�����O�ɊO�}���ā@�m�Łn���c���ؕ�
�@�@�@�܂��́A�m�Łn���i�P�{�S���f��sp�j1/2�|�P
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�Q���f��
�@
�@�@�@�@�@�@�@�@�@��sp�^���@���m�Łn�{���f�m�Łn�Q���@�{�E�E�E
�@�@�@�@�@�@�@�@�@�Z�x�̏������Ƃ���ł͋ߎ��I�Ɂ@�@�@�@�@�@�@�@�@�@�@�@
�@�@�@ �@�@�@�@�@�@�@�@�@�@��sp�^���@���m�Łn�{���f�m�Łn�Q��
�@�@�@�@�@�@�@���f�͒����̌X���ɔ�Ⴗ�閳�����̃p�����[�^�[�ŁAHuggins�̒萔
�@�@�@�@�@�@�@���f���O�D�R�`�O�D�U�Ȃ�m�Łn�̑���͐���
�D�{���S�x��inh���i�����@��rel�j�^���@�Ɓ@���@�̃O���t������B
�@�@�O���t�̌X�����|�i�P�^�Q�|���f�j�A�����O�ɊO�}���ā@�m�Łn���c���ؕ�
�@
�@ �@�@�@�@�����@��rel�^���@���m�Łn�|�i�P�^�Q�|���f�j�m�Łn�Q�@���{�E�E�E
�@�@�@�@�@ �����@��rel�^���@���m�Łn�|�i�P�^�Q�|���f�j�m�Łn�Q�@��
�@
�E�m�Q�i��sp�|�����@��rel�j�n�P�^�Q�^���@�Ɓ@���@�̃O���t������B
�@�@�O���t�̌X�����i���f�|�P�^�R�j�A�����O�ɊO�}���ā@�m�Łn���c���ؕ�
�@�m�Q�i��sp�|�����@��rel�j�n�P�^�Q�^�����m�Łn�{�i���f�|�P�^�R�j�m�Łn�Q�@���{�E�E�E
�@�m�Q�i��sp�|�����@��rel�j�n�P�^�Q�^�����m�Łn�{�i���f�|�P�^�R�j�m�Łn�Q�@��
�@
���Ɍ��S�x�m�Łn���m��sp�^���n�����O�͇B�C�D���疵�������悤�ɋ��߂�B
�FMark-Houwink-Sakurada�̎��@�m�Łn���j�E�l���@�@���@�l�@�����߂��T�j�B
�@�������A �j���T�D�S�T�~�P�O�|�S
�@�@�@�@�@�@�����O�D�V�R
�@
�Q�D�R�@�J���{���_���n�t���ł̕��������̍쐬
�@�@�s��������.�P�̂悤�ɃJ���{���_���n�t�P�O�O�O�����������B
�@�A�P���������ɂ��Q�T�O��������т�S�{��p�ӂ��A���ꂼ��Q�O�O�������ꂽ�B
�@�B�J���{���_���n�t��艷�����@���łP�O�O���ɂ�����A�|�����_�t�B�������e�т�ɂS�{�����ꂽ�B
�@�C�艷�����@���P�O�O���ɕۂ��A��莞�Ԍo�߂��ƂɎ���т̃|�����_�����ׂĎ��o���A����������Ƃ����B�P���������ɂ��A���o�����Ԃ̈قȂ�i��������x�̈قȂ�j�S��ނ̕����������B
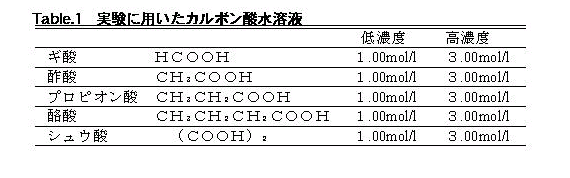
�Q�D�S�@�J���{���_���ł̕�������
�@�@�M�_�A�|�_�A���|�v���s�I���_�A���_�A���|�w�L�T���_���Q�T�O��������т�ɁA���ꂼ��Q�O�O�������ꂽ�B
�@�A�J���{���_�̓���������т��艷�����@���łP�O�O���ɂ�����A�|�����_�t�B�������e�т�ɓ���āA�ω����ώ@�����B
�@
�R�@���ʋy�эl�@
�R�D�P�@�J���{���_���n�t���ł̔S�x���ϕ��q�ʂƔj�f���x�̕ω�
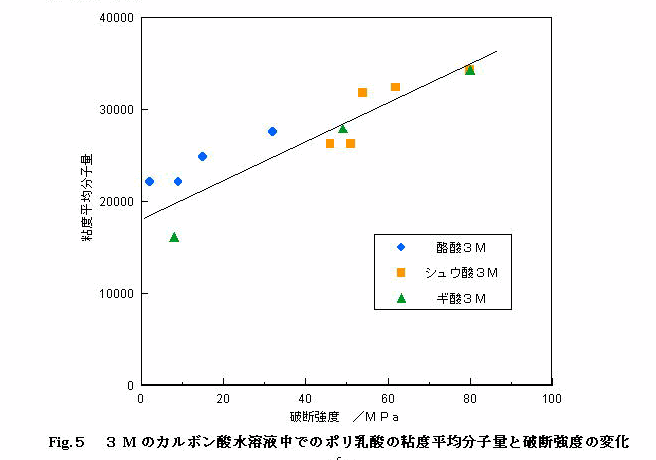
�@Fig.�T�͂RM�̃J���{���_���n�t���ł̃|�����_�̔S�x���ϕ��q�ʂƔj�f���x�̕ω������������̂ł���B�|�����_�̔j�f���x�̒ቺ�́A���q�ʂ̒ቺ�ƈ�v���Ă���B�܂�A�j�f���x�̒ቺ�Ƃ́A���q�ʂ̒ቺ�ł���A�|�����_�̉��������̐i�s�ł���B
�@
�R�D�Q�@�R�l�̃J���{���_���n�t�i�P�O�O���j���ł̔j�f���x�̌o���ω�
�@�R���g���[���Ƃ��ď������i�P�O�O���j���ɂR�O�O���Ԓu���ꂽ�|�����_�͕��ςV�W�D�X�l�o���̔j�f���x�������A��X�O�����̔j�f���x���ێ����Ă����B�@Fig.�U�́A�R�l�̃J���{���_���n�t�i�P�O�O���j���ł̃|�����_�̔j�f���x�̌o���ω������������̂ł���B���������ɔ�ׁA�J���{���_���n�t���ł̓|�����_�̔j�f���x���}���ɒቺ�����B�|�����_�̔j�f���x�̒ቺ�́A

�̏��ɑ����Ȃ��Ă���B�܂�A���n�t���̃J���{���_�̃A���L��������قǁA�|�����_�̉��������͑��i�����B�܂��A��ʂɁA���q�ʒቺ�͍����g�ƒ႐�g�ő��i������V�j�B�������A�J���{���_�̎_�𗣒萔�Ƃ��g��Table.�Q�̒ʂ�ŁA�����ɗp�����J���{���_�ł̓V���E�_�A�P���̃J���{���_�ł̓M�_���ł������_�ƂȂ邱�Ƃ���A�P�Ɏ_���x�������n�t�ł��邽�߂ɔj�f���x���ቺ�����Ƃ͂����Ȃ��B
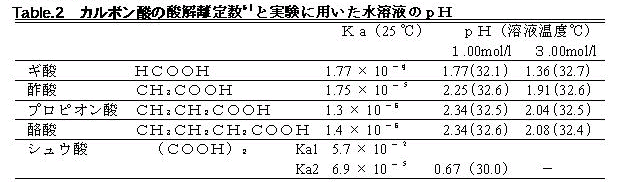
�R�D�R�@�Z�x�̈قȂ�J���{���_���n�t���ł̔j�f���x�̌o���ω�
�@
�@
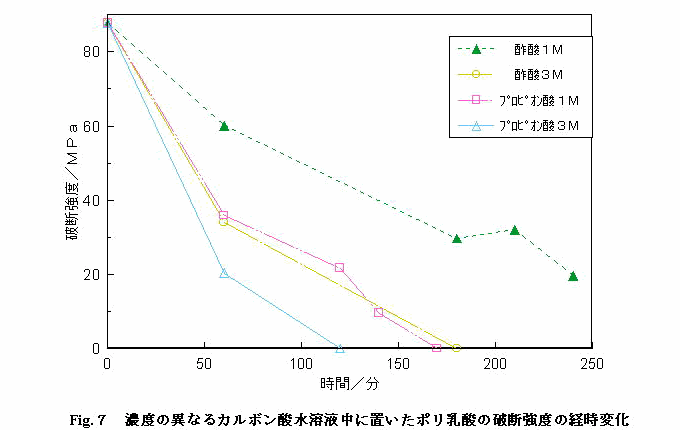
�@Fig.�V�͔Z�x�̈قȂ�J���{���_���n�t���ɒu�����|�����_�̔j�f���x�̌o���ω������������̂ł���B�����J���{���_���n�t�ł͍��Z�x�قǃ|�����_�̔j�f���x�͑����ቺ���Ă���B
�R�D�S�@�P���A�Q���̃J���{���_���n�t���ł̔j�f���x�̌o���ω�
�@
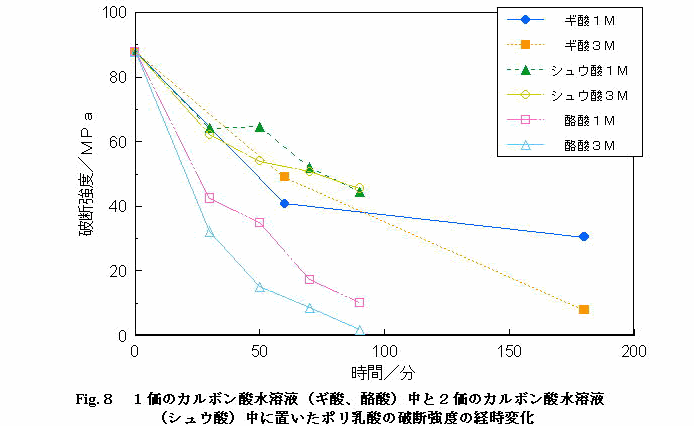
�@Fig.�W�͂P���̃J���{���_���n�t���ƂQ���̃J���{���_���n�t���ɒu�����|�����_�̔j�f���x�̌o���ω������������̂ł���B�|�����_�̔j�f���x�͂Q���̃J���{���_���n�t���ɒu���ꂽ���̂��P���̃J���{���_���n�t���ɒu���ꂽ���̂̕��������ቺ���Ă���B�܂�A�M�_�A�V���E�_�̂悤�ȃJ���{�L�V����ɃA���L������Ă��Ȃ��ꍇ�A�|�����_�̕����ɃJ���{�L�V����̉����͊W���Ă��Ȃ��Ƃ�����B
�R�D�T�@�J���{���_���ł̃|�����_�̕����i�n���j
�@�P�O�O���̃J���{���_�Ƀ|�����_��������s���������D�R�̂悤�ȕω����������B�܂��A��p����ƃ|�����_���͏o�����iFig.9�j�B
�@�J���{���_���̂ɕ���\�͂�����Ȃ�A�J���{���_�P�O�O���Ń|�����_������͂��ł���B�����āA���̕���\�͎͂������ʂR�D�Q�@���_���v���s�I���_���|�_���M�_�̏��ɂȂ�͂��ł���B�������A�J���{���_�ւ̃|�����_�̗n���́A

�ƂȂ�A�J���{���_�����n�t���Ŏ������|�����_�̕��𑣐i�x�Ɣ��̌X�����������B�|�_�͏o���A�v���s�I���_�͏o���̕��q�ʑ��肩��A�|�����_�͉�����������Ă��Ȃ����Ƃ������������A�J���{���_���|�����_�̉��������𑣐i����ɂ͐��n�t�łȂ���Ȃ�Ȃ��Ƃ������Ƃł���B���������āA�J���{���_���n�t���ł͑a�����̃A���L������͐e�����̃J���{�L�V����|�����_�̉��������ɒ��ڂ͂��炢�Ă���ƍl������B

�R�D�U�@�l�@
�@�������ʂ���A�|�����_�̉��������͐��n�t���̃J���{���_�̑��݂ɂ���đ��i����邱�Ƃ����������B���������̑��i�x�͐��n�t���̃J���{���_�̃A���L����̒����ɂ���ĈقȂ�A�A���L����̒��������������𑣐i�x���傫���B�������A�J���{���_���n�t�ł͂Ȃ��J���{���_�����̏ꍇ�̓A���L����Z�������|�����_�̗n�𐫂������A���������͋N����Ȃ��B�����n�t�̉������𑣐i�x�A�n�𐫂̈Ⴂ����A�|�����_�̐��n�t���ł̉��������ɉe����^���Ă���̂̓J���{���_�̃J���{�L�V����ł���A�J���{���_�̃J���{�L�V����̉������𑣐i�x�̓J���{���_�̃A���L����ɂ���Č��܂�ƍl������B
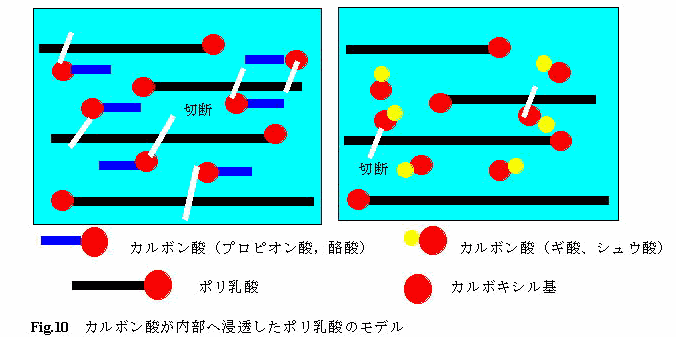
�@��ʂɁA�|�����_�͔�y�f�I�ȉ��������ɂ���Ēᕪ�q������B����́A���[�J���{�L�V����ɂ�鎩�ȐG�}�����ł���A�ᕪ�q�ʂقǕ��x�����܂�B�|�����_�̕��q���[�̃G�X�e�������́A���q�����̂��̂����P�O�{�����������������V�j�B���̂��Ƃ���A���n�t���ł̃J���{���_�̃J���{�L�V����ɂ��������𑣐i���ʂ�Fig.10�̂悤�ɁA�|�����_�����ɐZ�������J���{���_�̃J���{�L�V����|�����_���q���̖��[�J���{�L�V����̂悤�Ȍ��ʂ������āA�|�����_���q�����̃G�X�e�������������������Ă��邽�߂ł���ƍl������B�܂��A�|�����_�����ɐZ�������J���{���_�̃J���{�L�V����������𑣐i���ʂ��������߂ɂ́A�J���{���_�̃A���L�������������x�����K�v������B
�@
 �@
�@
�S�@���_
�@�|�����_�̉��������͐��n�t���̓K���ȃJ���{���_�̑��݂ɂ���đ��i�����B
�|�����_�̉������x�͐��n�t���̃J���{���_�̕����ʂ�A���L����̒����ɂ���ĈقȂ�B���ւ̗n��x�̑傫���J���{���_�̂����A�������𑣐i�x�̑傫���͎��̂悤�ɂȂ�B

�@
�T�@����̉ۑ�
�@����̓A���L����Ƀn���Q���Ȃǂ̓d�q�z�����̒u������������������s���A�J���{�L�V����|�����_�̉��������ɂǂ̂悤�Ɋւ���Ă���̂����������A�J���{�L�V����|�����_�̉��������𑣐i����@�\�̉𖾂�����ɂ����߂����B
�Q�l����
�P�j�y��@�`���ҁF�����𐫃v���X�`�b�N�̂��͂Ȃ��C���{�K�i����C�i1996�j
�Q�j�]���@���k�F�����𐫃|���}�[�̂͂Ȃ��C���{�H�ƐV���ЁC�i1995�j�@
�R�j�����_�э����w�Z���ȕ��F��P�U�w�N���u�������\��u���\�e�W�C���{���w��֓��x���C��.23�24�i1999�j
�S�j�����_�э����w�Z���ȕ��F�Q�n�������w�Z�_�ƃN���u�e�픭�\��\�_���i1999�j
�T�jA.Schindler and D.Hharpar,J.Polym.Sci.17,2593(1979)
�U�j�ێR�a���A��������A��J�W��A�����^���F�L�@���w�����Cp219�C���w���l�i1983�j
7�j�ҁ@�G�l�A���@�`�l�F�|�����_�Cp20�21�C�����q���s��C�i1997�j

�@�@�@

�@�@�@�@









 �@
�@